迄今为止,人们对古代青铜器自然腐蚀机理进行了大量研究,并根据其微观结构、表面形貌和形成机理对腐蚀产物进行分类和表征。以ROBBIOLA等[1-2]为代表的西方学者将青铜腐蚀分为两类:一类器物表面光滑致密,腐蚀层主要由含Cu、Sn元素的氧化物或氢氧化物组成,原有表面抛光和使用痕迹均被完全保留。另一类器物表面粗糙,形态、外观复杂,表面含有各类缺陷,如凹坑、蚀坑、气泡、结壳、裂隙等,此类器物具有三层腐蚀结构,最外层为土壤成分及二价铜的化合物,中间层为红色的Cu2O,内层为合金基体,基体中存在Cu元素流失,Sn元素富集以及Cl元素含量相对较高等现象。CHASE[3]认为这两类腐蚀分别对应于α相优先腐蚀以及δ相优先腐蚀。TAYLOR等[4]认为在海水环境中,青铜器的选择性腐蚀与环境中的含氧量有关。SCOTT[5]认为:α相与δ相哪一相优先腐蚀取决于氧的含量。SARAIVA等[6]认为在高含氧环境中,α相优先发生腐蚀;在低氧环境中,δ相优先腐蚀,金属铜重新沉积;这两种腐蚀现象可能出现在同一物体上,这可能是由于掩埋过程中环境发生变化,或受厚腐蚀层影响;在α与δ相中,铜流失为最主要的腐蚀现象。
国内学者同样从多方面研究了青铜器的选择性腐蚀。廉海萍[7]发现:α相优先腐蚀对青铜器破坏较小,已腐蚀的青铜虽已发生成分变化,但组织中仍保留了α树枝晶形貌;δ相优先腐蚀对青铜器破坏较大,此类腐蚀常会伴有纯铜晶粒析出;同一件青铜器在相同的埋藏环境中,由于表面结构不同,可能会发生不同类型的腐蚀。张予南等[8-12]均认为发生何种腐蚀取决于青铜器埋藏环境中的离子种类、含量,以及pH。王菊琳等[13-17]研究表明,青铜器在碱性环境中易发生钝化,在中性或弱酸性(pH5.4)土壤环境中,α相比δ相更易发生腐蚀。LI等[18]认为Sn含量和矿化腐蚀层中(α+δ)共析体的残留量对腐蚀起关键作用。GAO等[19]通过SKP试验证明α相比(α+δ)共析体活性更强,腐蚀应首先发生在α相中。
青铜器δ相优先腐蚀区中常伴有纯铜晶粒生成,DUNNE[20]发现纯铜组织会占据铅腐蚀后留下的空位以及铸造形成的气孔或缩孔。SMITH等[21-22]指出部分纯铜晶粒中存在孪晶结构,该结构取代了青铜器中的(α+δ)共析体。TYLECOTE等[23]认为铜晶粒析出是一种脱锡现象。WANG等[24]认为铜晶粒沉积需要在还原条件下进行,当铜离子或亚铜离子溶液饱和时,金属铜从溶液中沉积出来。EMAMI等[25]认为铜晶粒产生于金属晶界并以晶间腐蚀的形式扩展,腐蚀过程和随后的再沉积主要源于外层腐蚀产物生成时氧气耗尽,其次是由于埋藏环境中存在氯离子和氟离子。国内关于铜晶粒成因曾出现多种解释,如铸造时铜未完全溶解[26]、锈蚀引起的脱合金作用[27]、铜原子扩散理论等[28-29],后期学者多认为铜晶粒的形成与青铜器的电化学腐蚀有关[30-31]。
CHASE等[32-33]研究发现,大多数中国古代青铜器腐蚀由δ相开始,铜镜类器物腐蚀却多从α相开始。WANG等[34]发现,古铜镜基本内存在以铅皂为主的金属皂化物,此类物质耐蚀性极佳,会显著延缓基体腐蚀。笔者利用金相显微镜、扫描电镜能谱仪(SEM-EDS)分析山东地区青铜样品时,发现器物内同样普遍存在α相优先腐蚀与δ相优先腐蚀两种情况。铜镜类样品中α相优先腐蚀现象较为常见,此种腐蚀较为稳定;其他类型样品中δ相多已腐蚀,此种腐蚀对青铜器破坏较为严重。目前学界对于古代青铜器中为何出现选择性腐蚀的解释依旧较为模糊,为了更好地保护青铜文物,在对文物样品充分分析研究的基础上,通过电化学腐蚀原理及模拟腐蚀试验对青铜文物选择性腐蚀进行解析。
1. 试验
1.1 试验仪器
徕卡DM4P金相偏光显微镜,25 mm视野直径,透反射光观察。物镜倍数:50 X~1 000 X。
Phenom XL扫描电子显微镜,电子光学照明为CeB6灯丝,电子放大倍数100 000倍,分辨率≤15 nm。搭配美国EDAX公司Genesis 2000XMS型X射线能谱仪,能谱探测器能量分辨率<137eV。试验条件:真空度60 Pa,电压15 kV及配套电流。
普林斯顿PARSSTAT 4000A型电化学工作站,标配+/- 48V高槽压及+/- 4A大电流,最小电流量程40 pA,分辨率1.2 fA。配置10 μHz~10 MHz阻抗测试模块,1 μs高速采样。配有专业能源模块,专业腐蚀研究模块,标配电偶,电化学噪声等。
1.2 试样
山东地区青铜器普遍存在选择性腐蚀,受篇幅所限,本次列举的23件样品是自百余件器物中筛选出的典型器,详见表1,其中C、N、O等元素含量均已扣除。将试样打磨抛光后观察其剖面,试样未侵蚀、未喷碳/金。
2. 结果与讨论
2.1 样品分析
2.1.1 显微形貌分析
将α相优先腐蚀,仅δ相残留的情况称为①型腐蚀;δ相优先腐蚀,α相残留的情况称为②型腐蚀。①型腐蚀(图1)多出现在样品表层。②型腐蚀(图2)易向器物内部发展,有时贯通甚至布满整个器物。发生②型腐蚀的青铜器经常伴有橙红色纯铜晶粒生成。
部分器物同时存在两种腐蚀,见图3。在样品表层,δ相残留,α相完全腐蚀,为①型腐蚀。在样品内部或①型腐蚀区下方,α相残留,δ相完全腐蚀,腐蚀区内有橙红色圆形或不规则纯铜晶粒生成,为②型腐蚀。
2.1.2 扫描电镜及能谱分析
样品112-wbh中铅含量处于正常范畴,样品M32∶16为高铅青铜器,样品3240不含铅。青铜器是否含铅对选择性腐蚀并无实质性影响。因青铜腐蚀后主要表现为Cu元素流失及Sn元素富集,腐蚀相中铜锡含量可用于判断青铜器的腐蚀程度。
由图4和表2可见,在样品表层的①型腐蚀区中,δ相(32%Sn)基本未腐蚀,α相完全腐蚀(铜含量大幅度降低,其内有土壤元素溶入)。因α相中Cu元素流失严重,其内Sn、Pb元素相对含量均有所提升。
由图5和表3可见,三件样品基体中各元素含量均与理论值一致。在样品内部的②型腐蚀区,α相(80%~85%Cu,14%~16%Sn)未腐蚀。(α+δ)共析体中因Cu元素流失严重,锡质量分数由理论值的27%升至39%~50%,Cl离子含量略微升高。因(α+δ)共析体中流失的部分Cu离子会在青铜器铸造时形成的显微缩松或(α+δ)共析体及铅腐蚀流失后所遗留的空位中析出形成纯铜晶粒,青铜器基体与腐蚀区整体铜锡含量相差不大,铜含量仅略微降低。
图6(a)所示为3240号样品②型腐蚀区与未腐蚀基体交界处(左侧腐蚀,右侧未腐蚀),其内存在大量铸造时形成的显微缩松,腐蚀区域显微缩松部位已被铜晶粒填充,而基体部分依旧为孔洞状,能谱结果为缩松底部基体元素含量,见表4。
将图6(a)中5、6、7区域放大至10 000倍,以分析(α+δ)共析体内的腐蚀情况。图6(b)为(α+δ)共析体腐蚀前形貌,其能谱数据显示α相与δ相均未腐蚀,共析体中α相因过饱和固溶含锡量略高于基体中α相。图6(c)为(α+δ)共析体腐蚀过程中形貌,共析体左下方区域腐蚀程度较轻,右上方区域腐蚀程度较重;分析两侧元素,发现左下方区域δ相(32%Sn)未腐蚀,α相轻微腐蚀,相界(60%Cu,38%Sn)完全腐蚀;右上方区域δ相(24%Cu,64%Sn)完全腐蚀,α相轻微腐蚀,相界(50%Cu,49%Sn)完全腐蚀。图6(d)为(α+δ)共析体腐蚀后形貌,EDS结果表明δ相(25%Cu,74%Sn)完全腐蚀,共析体中仅α相残留。由此可知,δ相腐蚀后,Sn元素大部分在原位沉积,Cu元素则大量流失,这是②型腐蚀青铜器基体中Cu含量减少的主要原因。因(α+δ)共析体中存在大量相界,腐蚀初期以晶间腐蚀为主,腐蚀中后期为电偶腐蚀,δ相因牺牲阳极效应完全腐蚀,α相因阴极保护效应而残留。
2.2 模拟腐蚀试验
在①型腐蚀中α相为阳极,在②型腐蚀中δ相为阳极,青铜器选择性腐蚀本质上是一种电偶腐蚀。同一电偶在不同介质中会发生逆转,如Sn、Fe构成的腐蚀电池在水中时Sn为阴极,Fe为阳极,在有机酸中Sn为阳极,Fe为阴极。两种腐蚀出现在同一器物上说明外部环境一致,造成金相组织电位逆转的根本原因在于器物本身。
金属在土壤、海水、大气环境中易发生吸氧腐蚀,当青铜器表面光滑致密时,氧去极化反应在青铜表面均匀进行,腐蚀分布在整个金属表面,α相优先腐蚀,大阳极小阴极,对器物破坏较小。当青铜器表面粗糙,形态、外观复杂,表面含有各类缺陷,如凹坑、蚀坑、气泡、结壳、裂隙等时,在表面缺陷处易发生局部腐蚀(包括小孔腐蚀、缝隙腐蚀、电偶腐蚀和晶间腐蚀),腐蚀发生时因滞流关系,氧只能以扩散方式向表面缺陷处传递,氧消耗后难以得到补充,缺陷内、外构成氧浓差电池,形成了大阴极小阳极,腐蚀加剧。随着阴、阳极分化,腐蚀继续进行,二次腐蚀产物在缺陷口形成,此时缺陷内外组成的电池称为闭塞电池,见图7[35]。此类腐蚀阳极区面积很小,阴极区面积相对较大,导致金属表面上绝大部分处于钝性状态,腐蚀速率小到可以忽略不计,但在金属表面的缺陷区域,腐蚀速率很高,且会向金属内部发展,对器物破坏较大。
闭塞电池内溶液会发生很大变化,主要表现为pH降低和活性阴离子富集。青铜器闭塞区内腐蚀产生的金属离子水解会生成大量H+,造成闭塞区内介质pH下降,成为酸性很强的溶液;为了维持闭塞区内溶液的电中性,闭塞区外部溶液中阴离子会向闭塞区内迁移,当外部溶液中阴离子为Cl-或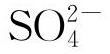 时,Cl-、
时,Cl-、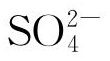 会扩散至闭塞区内部,形成强酸环境[35-36],若青铜器表面或内部存在金属皂化物,金属离子水解后产生的氢离子会优先将皂化物还原为有机酸,则仅会形成新弱酸环境。在强酸性的闭塞区内,锡的腐蚀产物SnO2不溶于酸,而铜离子在酸性环境中可溶,这应是造成②型腐蚀合金基体中Cu元素流失,Sn元素富集且Cl(或S)元素含量相对较高等现象出现的根本原因。
会扩散至闭塞区内部,形成强酸环境[35-36],若青铜器表面或内部存在金属皂化物,金属离子水解后产生的氢离子会优先将皂化物还原为有机酸,则仅会形成新弱酸环境。在强酸性的闭塞区内,锡的腐蚀产物SnO2不溶于酸,而铜离子在酸性环境中可溶,这应是造成②型腐蚀合金基体中Cu元素流失,Sn元素富集且Cl(或S)元素含量相对较高等现象出现的根本原因。
为验证青铜在中性及强酸性介质中的腐蚀情况,设计模拟腐蚀试验。将纯铜与纯锡混合后于熔金炉内熔化,浇筑为青铜饼。将青铜饼切割成尺寸规格相似的青铜条,分别用于充当电化学工作站的正负极。将电化学工作站的工作电极(WE)与第二参比电极(RE)并联接负极,辅助电极(CE)与第一参比电极(RE)并联后接正极,接地线悬空不接。因电化学工作站的正负极均为相同的青铜条,正负极间电压为零。此时使用电化学工作站腐蚀技术模块中的恒电位模式,在正负极之间添加恒电压(0.5 V),并将青铜样块接入电解质中。
青铜样块(1号)的锡质量分数约为17.5%,将正负极放入5%(质量分数,下同)氯化钠水溶液中,1.5 h后将青铜条取出,切割包埋并抛光,充当阳极的青铜条内部金相组织见图8。可以看到,在中性环境中,α相电位较低,优先腐蚀。保持电化学工作站设置不变,正负极更换为新的青铜条。为验证青铜器选择性腐蚀是否与Cl-或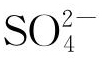 有关,选用了不含硫、氯的稀硝酸溶液作为强酸电解质。将正负极放入15%~20%稀硝酸电解质中,1.5 h后将青铜条取出,切割包埋并抛光,充当阳极的青铜条内部金相组织见图9。可以看到,在强酸环境中,δ相电位较低,优先腐蚀。
有关,选用了不含硫、氯的稀硝酸溶液作为强酸电解质。将正负极放入15%~20%稀硝酸电解质中,1.5 h后将青铜条取出,切割包埋并抛光,充当阳极的青铜条内部金相组织见图9。可以看到,在强酸环境中,δ相电位较低,优先腐蚀。
2号样块在15%~20%稀硝酸电解质中腐蚀后的微观形貌见图10,因其δ相相对面积较小,阳极样块腐蚀程度明显大于1号样块,腐蚀遗留的空位中有一定量的二氧化锡残留。比较奇特的是充当阴极的样块中也有少量δ相受到腐蚀(应为铜片放入强酸电解质中,未通电时造成的腐蚀),腐蚀遗留的空位被还原出的纯铜晶粒填满,该现象说明在强酸环境中腐蚀电池阴极会将溶液中的铜离子还原为纯铜,纯铜组织易在腐蚀遗留的空位中沉积。
2.3 纯铜晶粒成因
青铜器内腐蚀现象可通过Eh-pH图推导。依据CHASE等[37]绘制的Cu、Sn及其金属化合物Eh-pH图(图11),在低电位的还原环境中,Cu与Cu3Sn较为稳定;在高电位的氧化环境中,SnO2较为稳定,依据酸碱度不同,铜的稳定状态有Cu2+、CH2O5Cu、CuO、CuO2等。对于发生②型腐蚀的青铜器,闭塞区内pH呈酸性,α相因阴极保护作用电位降低,落在Cu(s)+Cu3Sn(s)稳定区,生成纯铜晶粒;δ相因阳极保护作用电位升高,落在Cu2++SnO2(s)稳定区,δ相中铜转变为Cu2+进入溶液,锡以SnO2形式原位沉积。
青铜器内各组织电位高低也可依据其在不同介质中的耐蚀性来判断,在闭塞区内α相耐蚀性高于δ相。发生②型腐蚀的青铜器中,当α相与δ相腐蚀殆尽时,腐蚀区存在大量纯铜晶粒残留,说明闭塞区中组织耐蚀性由大到小依次为Cu晶粒、α相、δ相。在闭塞区内,δ相为阳极,发生氧化反应,铜溶解进入溶液;α相为阴极,发生还原反应,将溶液中的阳离子还原为单质,当阴极附近铜离子富集时,铜离子被还原为单质铜。单质铜出现后,因电位较正,α-δ腐蚀电池会转变为Cu-δ腐蚀电池,新的单质铜会在纯铜晶粒表面生成,使纯铜晶粒长大(不排除腐蚀最初阶段α相中锡元素优先析出,在局部形成纯铜结构的可能性)。随着δ相腐蚀殆尽腐蚀电池转变为Cu-α腐蚀电池,α相开始腐蚀,这就是出现②型腐蚀的青铜器中,腐蚀区有大面积纯铜晶粒残留的主要原因。
85-01393号样品侵蚀后,铜晶粒中出现了明暗相间的孪晶结构(图略),孪晶仅在纯铜晶粒中出现,α相中无孪晶,可知该结构并非退火孪晶。近代工业中,精炼铜可以通过电化学方法实现,该方法将含有杂质的铜浇铸成阳极板,用纯铜薄片作为阴极片,相间装入电解槽中,用硫酸铜和硫酸水溶液作为电解液。在直流电作用下,阳极上的铜和电位较负的贱金属溶解进入溶液,贵金属和不溶金属成为阳极泥沉于电解槽底,溶液中的铜在阴极上优先析出,而其他电位较负的贱金属留于电解液中。②型腐蚀青铜器中闭塞区溶液同样为酸性,在不需要外加电流的情况下,电子会因电位差自发地由δ相流向阴极区,因此青铜器中纯铜晶粒的生成可以看作是一个天然的铜电解精炼过程。已知脉冲电沉积法可使电解析出的纯铜中出现孪晶结构[38],②型腐蚀青铜器内部,离子扩散速度缓慢,阳极与阴极之间电位差因浓差极化而时大时小,从而使腐蚀电池内电流时断时续,这为铜孪晶的形成创造了条件。
3. 结论
古代青铜器内存在α相优先腐蚀与δ相优先腐蚀两种情况。在一般的土壤、海水、大气等中性环境中,青铜器内α相电位较低,易发生α相优先腐蚀。但当其表面较为粗糙或外观复杂,含有各类缺陷时,在缺陷处易发生局部腐蚀,局部腐蚀使青铜内部形成闭塞区。闭塞区内金属离子水解使溶液酸化,pH降低造成金相组织电位逆转,此类青铜器中δ相优先腐蚀。为了维持闭塞区内溶液电中性,闭塞区外部溶液中阴离子向闭塞区内迁移,造成闭塞区内如硫、氯等腐蚀离子含量升高,此类腐蚀对青铜器结构破坏较大。
若器物表面较为光滑,表层α相优先腐蚀也有可能使金属局部产生缺陷或降低锈层中氧含量,进而诱发δ相优先腐蚀,此时两种腐蚀会出现在同一器物上,α相优先腐蚀在外,δ相优先腐蚀在内。在酸碱性不强的埋藏环境中,青铜器内产生何种腐蚀取决于器物内是否可以形成强酸环境。绝大多数青铜器表面较为粗糙,易形成强酸性闭塞环境,腐蚀多由δ相开始。古铜镜表面通常较为光滑,不易形成闭塞区,且铜镜内部或表面存在金属皂化物时,会在一定程度上避免酸性环境的形成,故铜镜内腐蚀多由α相开始。青铜器耐蚀程度取决于其内部腐蚀类型以及δ相与α相面积比。
在闭塞区内,青铜器不同组织间存在电位差,阳极发生氧化反应产生铜离子,阴极发生还原反应生成纯铜晶粒,因电解质溶液中离子扩散速度缓慢,腐蚀电池内部电流因浓差极化而时断时续,生成纯铜晶粒中有时会出现孪晶结构。
青铜器中腐蚀类型不同时应选用不同保护方法,内部仅α相优先腐蚀的器物状态较为稳定,不宜过度处理;内部存在δ相优先腐蚀区的青铜器必须使用倍半碳酸钠等碱性溶液浸泡,以中和闭塞区内酸性电解质,并置换腐蚀离子。
文章来源——材料与测试网













